Au cours du congrès sont présentées de nombreuses communications orales ainsi que des communications affichées sous la forme de "posters" qui permettent de discuter avec les auteurs plus directement. Le programme est généralement très dense, et c'était particulièrement le cas cette année à Prague. Pendant 4 jours se sont succédées des interventions sur des thèmes très variés tels que le transport et le stockage du fer, la régulation du métabolisme du fer, les différentes protéines du métabolisme du fer (on en connaît de plus en plus !), les modèles animaux de surcharge en fer, l'hepcidine, l'hémojuvéline, … et bien sur l'hémochromatose héréditaire.
Les points marquants du congrès 2005 sont l'impressionnante quantité de données scientifiques présentées et l'arrivée en force des modèles animaux (le plus souvent des souris) pour tenter d'expliquer les anomalies du métabolisme du fer observées chez l'homme.
Tout ceci demeure un peu abstrait pour les malades (et même parfois pour les médecins…). Sans minimiser l'importance des données scientifiques fondamentales, qui, si on ne perçoit pas toujours immédiatement leur intérêt, peuvent, à terme, apporter des améliorations notables pour la prise en charge des malades, essayons de voir quels sont, en pratique, les points à retenir.
- Après plusieurs années de flou, une classification plus claire des surcharges en fer héréditaires est en train d'apparaître (voir figures 1 et 2). Elle sépare les "vraies hémochromatoses" d'autres surcharges en fer (même héréditaires) qui ne s'expriment pas cliniquement de la même manière. Les gènes concernés par les hémochromatoses héréditaires sont maintenant bien connus : il s'agit pour les formes "adultes" des gènes HFE (de loin le plus important!) et TFR2 (récepteur 2 à la transferrine) et pour les formes "juvéniles" (plus précoces et sévères et fort heureusement beaucoup plus rares) des gènes de l'hepcidine et de l'hémojuvéline.
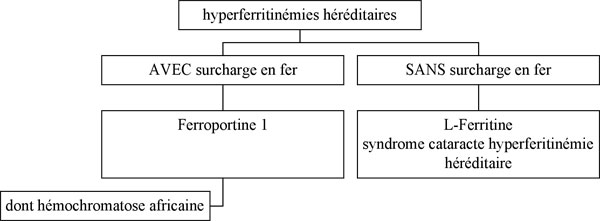
- D'autres maladies génétiques du fer sont maintenant connues, mais leur sévérité est bien moindre que celle de l'hémochromatose classique. Ce sont, par exemple les surcharges en fer par anomalie du gène de la ferroportine (une protéine qui fait sortir le fer des cellules).
- Ces classifications sont intéressantes et permettent d'y voir un peu plus clair ; cependant, on s'aperçoit que des anomalies de tous ces gènes peuvent parfois être associées chez certains malades, ce qui complique un peu les choses…
- Les études épidémiologiques montrent maintenant de manière formelle que le fait d'avoir une mutation ou des mutations sur le gène HFE ne "condamne" pas à évoluer vers une hémochromatose sévère. On savait déjà cela pour les homozygotes H63D où la maladie s'exprime très rarement, ou bien pour les hétérozygotes composites C282Y + H63D qui expriment une surcharge en fer le plus souvent plus modeste que les homozygotes. On sait maintenant que c'est également vrai pour les homozygotes C282Y: tous les homozygotes ne vont pas évoluer vers une surcharge grave. Ceci a pu être montré en suivant des sujets homozygotes sur de nombreuses années sans qu'ils ne développent de maladie. C'est donc un espoir pour les patients, et un argument supplémentaire pour ne pas préconiser de dépistage par le gène, mais par les tests biologiques de surcharge en fer (coefficient de saturation).
- Malgré les travaux en cours, il n'y a pour l'instant pas de progrès majeur dans les traitements des surcharges en fer et de l'hémochromatose. Au cours du congrès ont été présentées des études concernant des chélateurs (médicaments qui fixent le fer pour l'éliminer de l'organisme) oraux. Ces travaux sont encourageants, mais intéressent davantage les malades atteints d'anémies chroniques avec surcharge en fer (les thalassémies par exemple) que les hémochromatoses où les SAIGNEES demeurent le traitement de choix. Des travaux pharmacologiques très préliminaires sur l'hepcidine ont aussi été présentées mais n'ont pour l'instant aucune application pratique.
Le prochain congrès Bioiron aura lieu à Kioto (Japon) en 2007.
Patricia Aguilar Martinez-
Laboratoire d'hématologie, Hôpital Saint Eloi
Figure 1
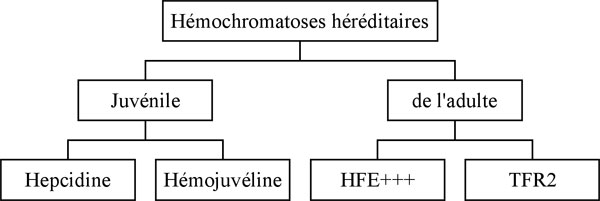
Figure 2
[1].actuellement le principal chélateur utilisé est injectable

